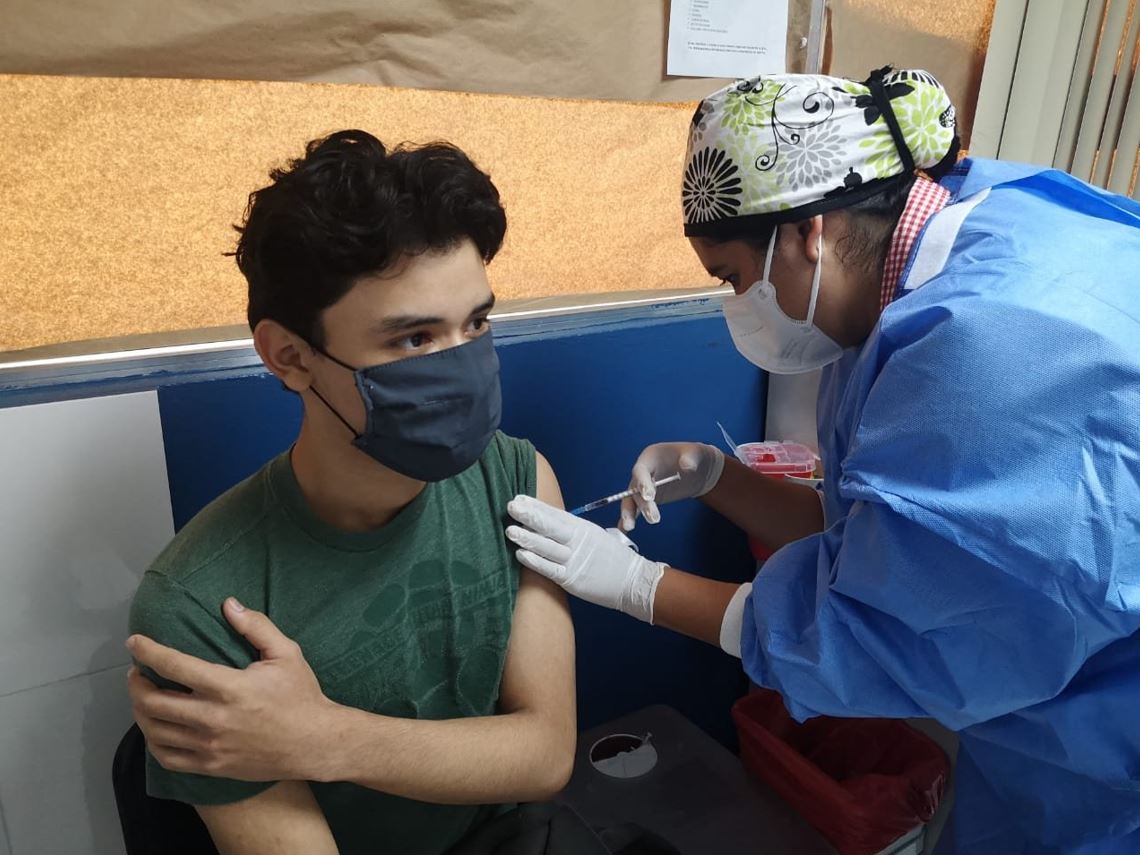
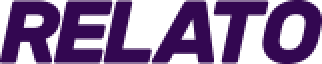La campaña de vacunación contra el COVID-19 para menores de edad ha sufrido retrasos. Los centros de atención instalados en todo el país resaltan por su falta de dosis de Pfizer, aprobada para el uso de los más jóvenes.

Solo habían ingresado 533 mil 520 dosis destinadas para los menores entre 12 y 17 años. Sin embargo, el Instituto Nacional de Estadística (INE) contempla que son cerca de 2 millones 121 mil 284 menores los que conforman este grupo. Para finales de octubre, los centros de vacunación ya anunciaban que contaban con muy pocas dosis de Pfizer para aplicar por día y, posteriormente, la escasez total.
El presidente Giammattei había afirmado el 12 de noviembre que se adquirieron hasta 2.5 millones de dosis de esta farmacéutica por medio del mecanismo COVAX para continuar vacunando a menores y este 15 de noviembre, un primer lote arribaría al país. Sin embargo, el ministro de salud Francisco Coma informó que “un problema de logística” provocó un retraso y la llegada de las deseadas dosis estaba indefinida.
Sin vacunas que utilizar, el Ejército de Guatemala informó que el 13 y 14 de noviembre utilizarían hasta 4 mil vacunas de Moderna para poder inocular a menores de entre 12 y 17 años dentro de los puestos de vacunación de Mariscal Zavala y Guardia de Honor. Según el portavoz de la institución, Rubén Téllez, estas habían sido autorizadas por el MSPAS, recordando que no se podían combinar las vacunas de Pfizer y Moderna.
Sin embargo, la decisión de las autoridades resaltaron las aprobaciones y usos de vacunas de COVID-19 para menores de edad en otros países. En Estados Unidos, la única vacuna aprobada por los Centros para el Control y la Prevención de Enfermedades (CDC por sus siglas en inglés) es la de Pfizer. Incluso, dentro de su portal web, recomienda que no se usen dosis de Moderna para inmunizar a menores de 18 años.
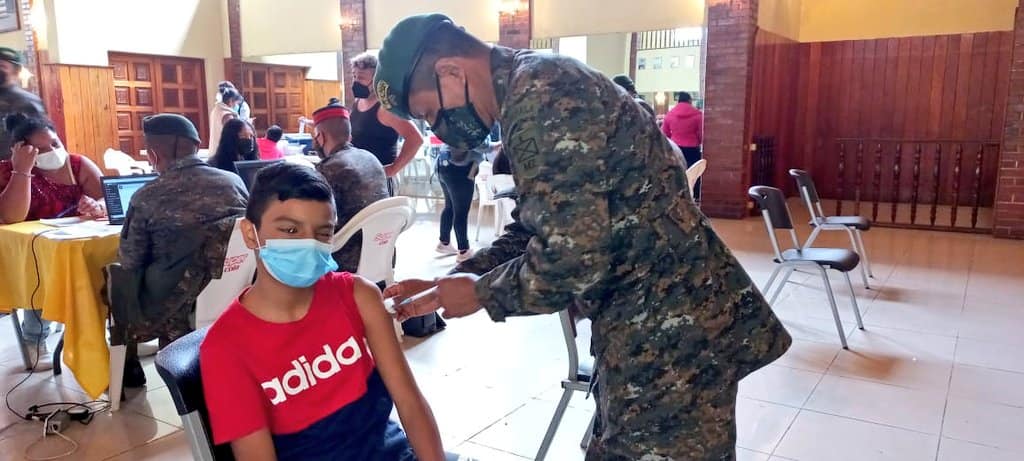
La farmacéutica Moderna ya había realizado estudios exitosos donde los menores que habían utilizado su vacuna habían resultado protegidos contra el virus. Pero, hasta la fecha, solo la Agencia Europea de Medicamentos (EMA) ha brindado la autorización para su uso de emergencia, pero no se ha aprobado ninguna extensión. Aún se evalúa la posibilidad de utilizarla en menores de 11 años.
El pasado 31 de octubre, la Administración de Alimentos y Medicamentos de Estados Unidos (FDA por sus siglas en inglés) demoró su decisión sobre aplicar dosis de Moderna en niños entre 12 y 17 años para protegerlos contra el COVID-19 debido a un “inusual riesgo de inflamación cardíaca que la vacuna puede provocar.”
Según Moderna, hasta octubre de 2021 han sido vacunados más de 1.5 millones de adolescentes en todo el mundo, donde el riesgo de inflamación no ha sido una razón para alarmar a las autoridades de otros países.